今回はルイス酸・ルイス塩基について解説します。ブレンステッド・ローリーの酸・塩基と何が違うのか、見ていきましょう!
ブレンステッド・ローリーの定義について知りたい方はこちらをご覧ください。
ルイス酸・ルイス塩基の定義
まずは定義の確認をしましょう。
ルイス酸とは…電子対を受け取る物質
ルイス塩基とは…電子対を与える物質
つまり、電子対の受け渡しが関係していることがわかります。
ルイス酸・ルイス塩基のメリット
ブレンステッド・ローリーの定義は水素イオンの受け渡しが関係してましたね。
ルイス酸・ルイス塩基の考え方を用いると水素イオンが関わっていない反応も考えることができます。
ブレンステッド・ローリーの定義との比較
ブレンステッド・ローリーの定義とルイス酸・塩基を比較すると受け渡しするものがあるという点が同じです。
また、ルイス酸は電子対を受け取るので陽イオンであることも多く、ルイス塩基は電子対を与えるので陰イオンであることも多いです。
このことから、酸から塩基には正の電荷が移動し、塩基から酸には負の電荷が移動するという点でも同じですね。
ルイス酸・塩基の具体的な例
言葉での説明は以上にして、具体的なルイス酸・塩基の例を見てみましょう。
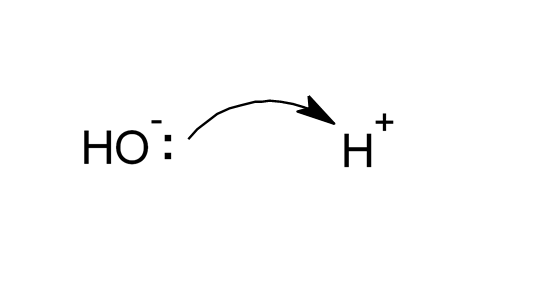

電子対を受け取るルイス酸が水素イオン、電子対を与えるルイス塩基が水酸化物イオンとなっていますね。
もう一つ見てみましょう。
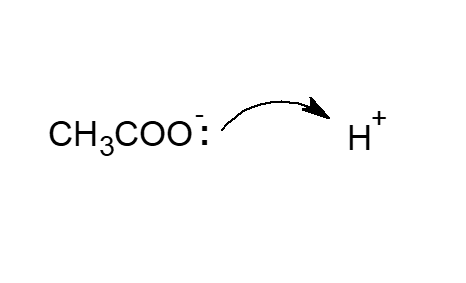

酢酸イオンがルイス塩基、水素イオンがルイス酸ですね。
ここまではブレンステッド・ローリーの定義でも説明できる酸・塩基ですね。
陽イオンと陰イオンの反応以外では以下のようなものもあります。
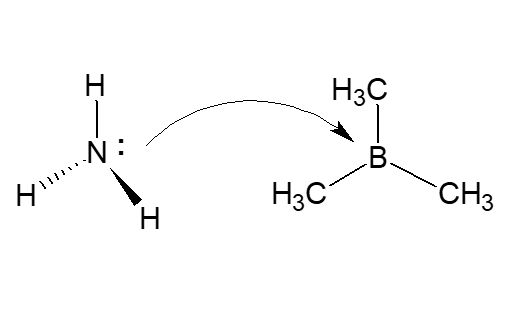

水素イオンがありません!でも、ルイス酸・塩基の定義からアンモニアがルイス塩基、トリメチルボランがルイス酸となりますね。
以上です。最後まで読んでいただきありがとうございました!




コメント