「硬い酸、塩基」「やわらかい酸、塩基」といった表現について今回は解説したいと思います。「Hard酸、Hard塩基」などとも言いますね。
HSAB則とは?
酸・塩基についてはブレンステッド・ローリーの定義やルイス酸・ルイス塩基の定義がありますね。
酸塩基の反応のしやすさについてはブレンステッド・ローリーの定義では平衡定数があります。
しかし、ルイス酸・ルイス塩基の反応のしやすさはどのように決めるのでしょうか?
その答えの1つにHSAB則があります。
HSABとはhard acid、hard base、soft acid、soft baseの略です。硬い酸・塩基、やわらかい酸・塩基、hardな酸、softな酸などとも言われます。
酸・塩基の「hard・soft」はどういう意味なの?
HASB則は酸塩基の反応のしやすさを考えるために導入するんでしたね。
どのようにして反応のしやすさが決まるのでしょうか?
まず、hardな酸塩基は分極しにくく、softな酸塩基は分極しやすいことを表します。
つまり、外部の電場により原子核の周りの電子分布が変形しにくいとhard、変形しやすいとsoftと分類できます。
イメージとしてはこんな感じです。(あくまでイメージです、正確な図ではないです)
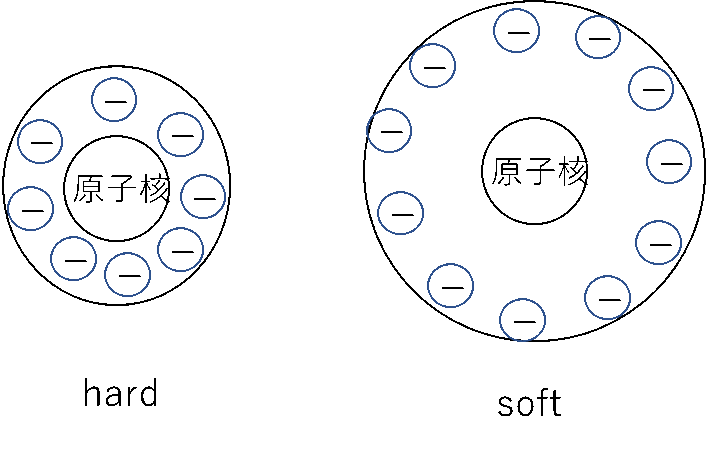

hardな酸塩基は原子半径が小さく、原子核に強く引き付けられています。よってプラスの電荷が近づいてきても分極しにくいです。
softな酸塩基は原子半径が大きく、原子核から引き付けられる力が弱いです。よってプラスの電荷が近づくと分極しやすいです。
HSAB則で反応しやすいのはどういうとき?
hard、softの意味がわかったので次はどのようにして反応のしやすさが決まっているかを解説します。
まず、HASB則では「hard同士、soft同士で強い結合を作る」と覚えておいてください。
強い結合を作るということは結合しやすい、つまり反応しやすいということです。また、水に溶けにくいなどの性質も示します。
よって、反応しやすい組み合わせは以下の通りです。
- hardな酸とhardな塩基
- softな酸とsoftな塩基
逆にhardな酸とsoftな塩基などの反応だと結合しにくく、水に溶けやすいなどの性質を示します。
hard酸・塩基、soft酸・塩基の分類
どんなときに反応しやすいかがわかったのでhard、softがどのように分類されるかも知っておきましょう。
hardな酸塩基に分類されるのはどんなとき?
基本的にはhardに分類されるのは以下のようなときです。
- 原子半径が小さい
- 負の電荷が小さい
原子半径が小さいときは電子が原子核に近く、陽イオンなどが近づいてきても分極しにくいんでしたね。
負の電荷が小さいと、原子核が電子を引き付ける力が相対的に強くなるので分極しにくくなります。
softな酸塩基に分類されるのはどんなとき?
こちらも基本的にはsoftに分類されるのは以下のようなときです。
- 原子半径が大きい
- 負の電荷が大きい
原子半径が大きいときは電子が原子核から離れており、陽イオンなどが近づいてくると分極しやすくなりますね。
負の電荷が大きいと、原子核が電子を引き付ける力が相対的に弱くなるので分極しやすくなりますね。
hardな酸・塩基、softな酸・塩基の例
hardな酸
硬い酸は一般的に
H+、Li+、Na+、K+、Ca2+、Mg2+、Al3+、Cr+、BF3
などです。
softな酸
Cu+、Au+、Ag+、Hg2+、Pt2+、Fe
などがあります。
hardな塩基
F–、Cl–、OH–、SO42-、NH3、NO3–
などがあります。
softな塩基
H–、CN–、I–、S2-、CN–、CO
などがあります。
hardな酸・塩基、softな酸・塩基の例から言えること
これらの分類を見ると以下のことがわかります。
・1つの族に注目すると周期表の下にいくほど軟らかくなる
これは下にいくほど原子半径が大きくなるからですね。
・hardな原子が結合していると硬い
例えばNO3–はhardな塩基ですがこれは硬い原子であるO2-が結合しているためです。
・炭素原子が結合していると軟らかい
COやCN–はsoftな塩基ですね。
また、錯体ではルイス酸は金属、ルイス塩基は配位子になるのでそこを意識すると考えやすいかもしれません。
まとめるとこんな感じです。
- hardな酸塩基は分極しにくく、softな酸塩基は分極しやすい
- hard同士、soft同士で強い結合を作る
- 1つの族に注目すると周期表の下にいくほど軟らかくなる
- hardな原子が結合していると硬い
- 炭素原子が結合していると軟らかい
以上です!最後まで読んでいただきありがとうございました!




コメント