今回はNMRの原理についてです。
NMRの原理といえば、大学院の口述試験で聞かれるとの噂もあります。
私も実際に聞かれたという話を聞いたことがありますし、筆記試験や学生実験のレポートで問われることもありますよね。
復習したい方、原理についてサクッと知りたい方向けにこの記事を書こうと思いました。
読み終わる頃には、遮蔽効果による「高磁場シフト」や「低磁場シフト」などの呪文の意味を自分で説明できるようになります!つまり、下の図の意味とその原理が理解できると思います!

ちなみに私は大学院入試のときに以下の本で勉強しました。合成の実験をするようになってからも頻繁に見返せる本としておすすめしておきます。
それではやっていきましょう!
追記:最近カップリングについても記事にしたので気になる方はチェックしていただけると嬉しいです!
NMRとは?
この記事では主に1H NMR分光法を対象とします。
1H NMR分光法では、有機化合物に必ずと言っていいほど含まれる水素原子を対象とします。試料中の水素原子が置かれている環境が異なることを利用して、試料がどんな構造をしているのかを調べます。水素原子が置かれている環境というのは、例えばトルエンだとメチル基の水素と芳香環の水素の環境が異なるということです。
NMRの原理
NMR分光法では化合物と電磁波の相互作用を利用して構造解析します。この点では赤外分光法や紫外・可視分光法と同じですが、NMR分光法に特徴的なのは磁場をかけて、電磁波を照射することです。なぜ、磁場をかけるのでしょうか?
核磁気モーメント
磁場をかける理由は、NMR分光法(ここでは1H NMR)では水素原子の原子核に存在する核スピンを観察しているからです。水素原子核には一個の陽子があり、正電荷を持っています。

水素原子核は自転運動していることが知られており、これは核スピンとも呼ばれます。これにより水素原子核は小さな磁石の性質を持ちます。原子核は正の電荷を帯びているため、これが回転すると、磁場が発生する、というのは高校でも習う「電流の周りに磁界が発生する」ことからも理解できますね。この磁石としての強さは核磁気モーメントと呼ばれます。
(ちなみに核スピンを有する原子核は、原子番号と質量数のいずれか、あるいは両方が偶数ではないものです。そうでないものではNMR分光法の対象にはなりません。これは、原子核内で陽子と中性子が他の陽子、中性子同士とスピン対を形成することに由来するらしいです。陽子と中性子のどちらか一方でも奇数だと、核スピン量子数が0にならないため、NMR測定が可能になります)
核磁気モーメント・・・原子核が持つ磁気モーメントのこと。磁気モーメントは磁石としての強さを表すベクトル量
式としては以下のような形をしています。
\[\mu=\frac{h \gamma}{2 \pi} I\]
hはプランク定数、Iは核スピン量子数で1H核では1/2です。γは磁気回転比と言って1H核の場合は42.58 MHz/T、13C核では10.71 MHz/Tと言ったように原子核によって異なる値です。
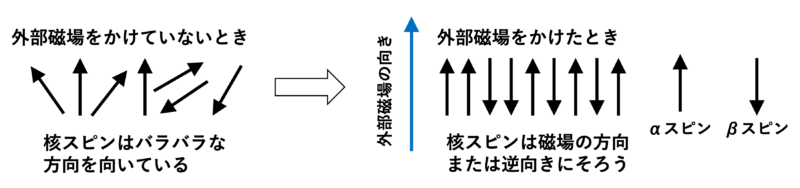
核磁気モーメントは量子化された値であり、連続的ではない飛び飛びの値を持ちます。つまり、外部磁場をかけると、その方向と同じ向きのαスピンと逆向きのβスピンという2つの状態が考えられます。ここでエネルギー的に安定なのは磁場と同じ向きのαスピンです。とはいえエネルギー差は非常に小さいので、ボルツマン分布からαスピンとβスピンの数の比を求めても0.01%程度の差です。

ゼーマン分裂・共鳴周波数
外部磁場Bに1H核が置かれるとμBと-μBの2つのエネルギー準位に分裂します。この分裂はゼーマン分裂と呼ばれます。
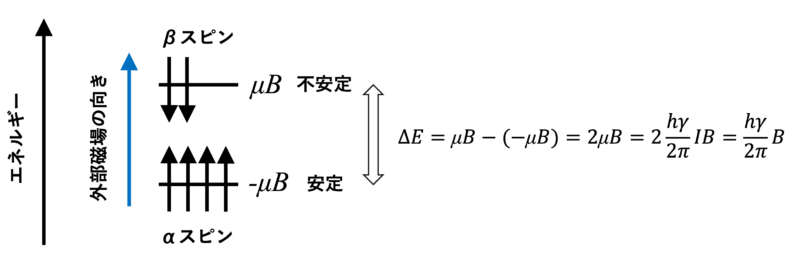

したがって、このエネルギー差は以下の式のようになります。Bは外部磁場の強さです。
\[h \nu=\frac{h \gamma}{2 \pi} B\]
つまり、ΔEに相当するエネルギーの電磁波を照射すると、安定なαスピンからβスピンへの遷移が起こります。以下の式のように電磁波のエネルギーhνから、吸収される電磁波の周波数が求まります。これは共鳴周波数と呼ばれ、αスピンとβスピンのエネルギー差ΔE はラジオ波の領域に相当します。その後、ラジオ波の照射を止めると、ラジオ波を吸収したことにより高いエネルギー準位にあった原子核がエネルギーを放出しながら元の状態に戻っていきます(この過程は緩和とも呼ばれます)。この放出されたエネルギーを電気信号として捉えて、私たちがよく見るNMRスペクトルとして出力されます。
共鳴周波数・・・ゼーマン分裂を引き起こす際の周波数のこと。以下の式で表される。
\[\nu=\frac{\gamma}{2 \pi} B\]
よく400 MHzや600 MHzなどのNMR装置の性能を表す言葉を聞きますが、これらは共鳴周波数のことです。基本的には1H核の共鳴周波数が装置の性能を示す際に使われます。ちなみに、ゼーマン分裂が大きいほどNMRスペクトルの感度が良くなります。したがって、外部磁場の大きい装置を使う方が綺麗なスペクトルが得られます。600 MHzのNMR装置を使った方が400 MHzの装置よりも綺麗な(分解能の高い)スペクトルが得られるのはこういった理由です。磁気回転比γの大きな核種を使うと感度が良くなることも上の式で説明できますね。
化学シフト・遮蔽効果
ここまで見てきたように、1H核は外部磁場を照射すると、αスピンとβスピンに分裂し、外部磁場の大きさに依存した、共鳴周波数を持ちます。このままだと有機化合物に含まれる1H核は全て同じ共鳴周波数を持つことになり、ラジオ波を照射しても一本のピークしか観察されないように思います。しかし、同じ1H核でも置かれる環境によってわずかに共鳴周波数が変わるのです。これを化学シフトと言います。
化学シフト・・・同じ核種でも化学構造の変化にともなって共鳴周波数に違いが出ることを化学シフトという。
これによって、化合物に固有のスペクトルが得られるので、構造決定ができるという訳です。
では、1H核の置かれる環境によって、なぜ共鳴周波数が変わるのでしょうか?
1H核の周辺に置換基や特定の化学構造があると、1H核の周りの電子密度が変化します。このような環境の違いが化学シフトを生み出しています。もう少し具体的にお話ししましょう。
1H核周りの電子は自由に動くことができます。原子核が感じる磁場は、分子内の他の原子が持つ電子によって生じる磁場に影響されます。このような他の原子中の電子によって生じる磁場は局所磁場と呼ばれます。
外部か外部から磁場をかけると、電子の動きが誘起され、外部磁場とは逆向きの局所磁場が生じます。局所磁場が大きいほど、実際に1H核が感じる磁場は小さくなります。
これは遮蔽効果と呼ばれ、1H核の周りの電子密度が高いほど、遮蔽効果は大きく、共鳴周波数は小さくなります。一方、電子密度が低いほど、遮蔽効果は小さくなり、共鳴周波数は大きくなります。遮蔽効果によって、NMRスペクトルには分子構造や結合状態に依存したピークが現れて、私たちは構造決定に関する情報を得ることができます
局所磁場によって1H核が感じる磁場の変化は遮蔽定数σを用いて、
\[B_{\mathrm{loc}}=B_{0}-\sigma B_{0}=(1-\sigma) B_{0}\]
と表せます。
これにより、共鳴周波数は以下の式ように変化します。つまり、共鳴周波数が1H核の置かれる環境によって変わり、これによって特徴的なピークが現れ、分子構造を解析できる、と理解しておきましょう。
\[\nu=\frac{\gamma B_{\mathrm{loc}}}{2 \pi}=\frac{(1-\sigma) \gamma B_{0}}{2 \pi}\]
化学シフトと横軸の関係【δ/ppmとは?】
化学シフトの原理はわかりましたが、実際には共鳴周波数の変化とピークの位置はどのような関係なのでしょうか?
まずはNMRスペクトルの横軸について知る必要があります。一般的なNMRスペクトルだと縦軸はシグナル強度比ですが、横軸はδ/ppmで表されます。なぜ、NMRスペクトルの横軸はδ/ppmなのでしょうか?
照射するラジオ波の周波数はNMR装置の外部磁場に依存します。つまり、400 MHz、600MHzなどと装置が変わった際にも比較できるような基準を定めないといけません。
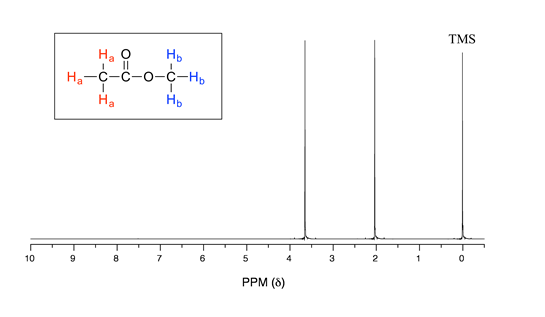

NMRスペクトルの横軸はδ(ppm)がよく用いられ、これは測定された共鳴周波数から、あらかじめピークの位置が判明している標準物質(基本的には以下で説明するTMSが用いられる)の共鳴周波数を差し引き、使用した周波数で割った値です。NMR装置の周波数は数百MHzなので、δはppm(百万分の1)オーダーになります。
上に示したNMRスペクトルを見ると0 ppm付近にTMSと書かれていますね。これが標準物質です。TMSとはなんでしょうか?以下で説明します。
高磁場シフト・低磁場シフト・TMSとは何か?
TMSとは何者かをお話しする前に、低磁場、高磁場について説明しておきます。
NMRスペクトルの左側は低磁場、右側は高磁場と呼ばれます。つまり、先ほどのNMRの図で言うと、0 ppm側が高磁場です。NMRの測定中は外部磁場の大きさは固定されるのですが、電磁波の周波数も固定する場合、吸収する電磁波の周波数が大きいほど外部から強い磁場をかけて電磁波に相当するΔEに近づける必要があります。そのため、慣習的に右側が高磁場と呼ばれるのです。
先ほど、NMRスペクトルの横軸には標準物質によって決定されることをお話ししました。1H NMRにおける標準物質は基本的にテトラメチルシラン (TMS)でして、TMSのメチル基のピークが0 ppmになるようにします。分子構造を以下に示します。TMS中のCH3の部分は全て同じ環境下にあるので、ピークとしては1つしか観測されません。
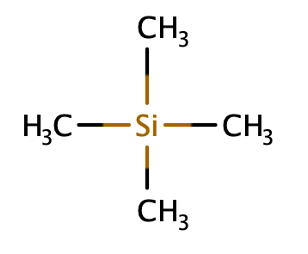

TMSはSiの電気陰性度がCより小さいため、Si+C-のような分極が生じます。これにより、CH3の1H周辺の電子密度が大きくなり、通常の有機分子よりも高磁場側で共鳴します。まとめると最初に示した以下の図のようになります。


アルコールやカルボン酸などのOHのピークはよく低磁場側に現れます。これは電気陰性度の高いOに電子が引き寄せられ、1H核に対する遮蔽が小さいため、TMSを基準にすると真逆の低磁場側にピークが現れるのです。
まとめ
さて、ここまででNMRの原理を説明してきました。まとめると、
- NMR分光法では核スピンを測定している。核スピンに磁場をかけると、磁場と同じ向きのαスピンと逆向きのβスピンという分類ができ、このエネルギー差に相当する電磁波がラジオ波である。
- 1H NMRにおいて、化学シフト値は主に水素原子核の周辺の電子密度の大小で決まる。
- 化学シフト値はTMSのメチル基の共鳴周波数を0とし、これと測定された共鳴周波数との差を測定周波数で割った値である。
一度で理解できなくても、参考書などと合わせて何度も読み返せば徐々に理解できるはずですので、頑張りましょう!最後までご覧いただきありがとうございました!
Noteで化学系就活のことや、研究生活のことなど書いているので覗いてもらえるとうれしいです!


・本記事で紹介したおすすめの参考書↓
他のNMRに関する記事も書いているのでもっと詳しく知りたい!と言う方は見ていただけるとうれしいです!
※本記事のサムネイルはかがくイラスト様の素材を使わせていただきました。





コメント